2020年,一名36岁的巴西男子上了世界各地的头条,因为他是第一个使用一种容易获得且耐受性良好的鸡尾酒药物被推定治愈人类免疫缺陷病毒(HIV)的人。
艾滋病毒治疗领域令人心碎地充斥着最初宣布治愈的患者,他们最终看到自己的感染复发。可悲的是,这个病人的治疗最终也是如此。但是,他的病例播下了谨慎的希望,也许,只是也许,我们离治愈的道路又近了一步。
最令人兴奋的是,这位
BMT是一项不小的努力。它包括清除原有的免疫系统(包括,希望包括所有感染hiv的细胞),并用健康的供体细胞重新播种。这是一种刀耕火种的方法,大致相当于摧毁并再生一个器官。柏林和伦敦的患者被植入了来自捐赠者的细胞,这些捐赠者缺乏HIV的主要细胞表面共受体,C-c趋化因子受体5型(CCR5),这意味着他们的“新”免疫系统将免受r5型病毒感染。
骨髓移植成本高、风险大、手术密集,对数百万艾滋病毒感染者来说不是一种可扩展的选择,尤其是在资源匮乏的地区。然而,一种容易获得的药物鸡尾酒可能就是这样。
HIV潜伏期和寻找治疗方法的困难
尽管抗逆转录病毒疗法(ART)取得了巨大的成功,在大多数坚持治疗的个体中,它将病毒复制控制在低水平或无法检测到的水平,但真正治愈艾滋病毒一直是难以捉摸的。这是由于艾滋病毒的潜伏期,在这种情况下,病毒隐藏在长寿的宿主细胞(如静止记忆T细胞)的基因组中,处于非活性状态,从而逃避免疫清除。由于抗逆转录病毒疗法作用于病毒复制机制,不积极复制的潜伏病毒也会躲避抗逆转录病毒药物。
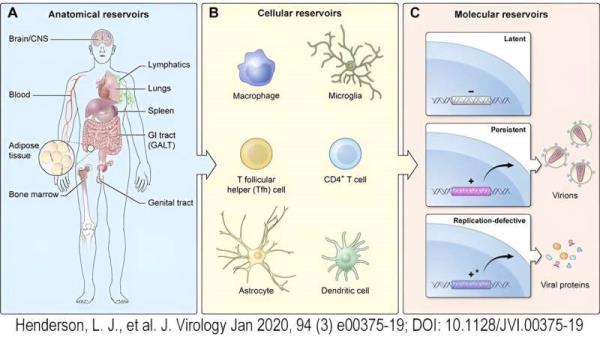
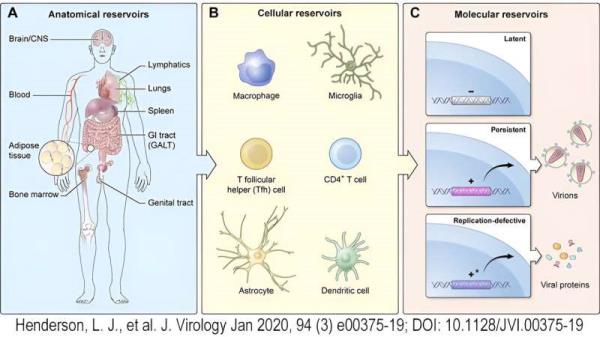
多年来,科学家们已经认识到,在寻求治疗方法时,潜伏期是需要克服的主要挑战之一。虽然长寿命的静止中枢记忆CD4+ T细胞是潜伏HIV的主要储存库,但已知它也可以在各种其他CD4+ T细胞区室、巨噬细胞甚至树突状细胞中建立潜伏感染。
潜伏感染的细胞也可能隐藏在特殊或复杂的解剖部位,如中枢神经系统、生殖道或肠道相关淋巴组织。除了使治疗策略复杂化之外,这些病毒储存库使确定病毒是否留在体内变得困难,因为许多临床研究只在循环免疫细胞中检测病毒前DNA,而这些细胞可以在标准抽血中收集。更重要的是,就像癌症一样,只需要一个缺失的储存细胞就能重新引发感染。
鉴于这些挑战,许多研究小组正在研究分子方法,以诱使艾滋病毒从隐藏的地方出来,进入免疫系统的视野。驱动HIV的表达是可取的,因为它使病毒成为正常免疫机制破坏的目标,并且希望这样做将导致清除潜伏库。
近年来进行了许多使用潜伏期逆转剂(LRAs)的试验。这些方法必须达到微妙的平衡,既要引起足够的免疫激活,释放全部隐藏的原病毒库,又不能过度激活免疫系统,导致脆弱部位(如大脑)发炎。不幸的是,一项体外研究表明,即使100%的T细胞亚群被激活,一些完全有能力的原病毒仍然被隐藏起来。
这表明单独的细胞激活作为一种潜伏期逆转策略可能不足以清除病毒库。
另一个焦点集中在HIV潜伏期的表观遗传学上:换句话说,试图消除转录抑制,这样HIV就可以在不过度激活免疫系统的情况下表达。
这一武库中的一些策略包括转录因子,如活化B细胞的核因子κB轻链增强剂(NF-κB)或活化T细胞的核因子(NFAT),促进病毒表达,组蛋白去乙酰化酶(HDAC)抑制剂,有助于放松DNA,使其可以转录,甲基转移酶抑制剂,去除HIV启动子中的抑制酶活性。
基因编辑策略也被尝试过。这些疗法的重点是改变细胞基因组,而不是驱动病毒表达,从而促使免疫系统自然地消灭受感染的细胞。在动物模型的临床前研究中,使用锌指核酸酶破坏CCR5共受体基因显示出对HIV有希望的保护作用,但到目前为止还不能治愈。随后的临床试验对这种方法进行了评估,结果表明这种方法是安全的,足以减少HIV病毒血症,但它们并没有最终导致HIV治愈。
聚类规则间隔短回文重复(CRISPR)-Cas9基因编辑方法也在临床前进行了广泛的研究,在针对HIV gag基因的组合方法中取得了一些成功,并在小鼠模型的多个体室中消除了病毒检测。
然而,这种疗法在7只老鼠中有2只成功,尚未进行临床试验。最近的一项人类病例研究显示,在一名患有合并症白血病的HIV患者中,CRISPR破坏CCR5的情况仅显示出有限的植入。尽管如此,基因编辑策略仍然是未来艾滋病毒研究的有希望的方法。
当涉及到消除威利艾滋病毒储存库时,多种策略的组合可能是游戏的名称。尽管已经研究了许多HIV清除策略,但在临床中,没有一种策略在病毒清除与方案耐受性之间取得了相当好的平衡。然而,将几种策略结合在一起仍然有很大的希望,而这正是
圣保罗病人的治疗
Ricardo Diaz医学博士和他在
- 的有限公司对照组坚持常规ART治疗方案。
- 另一组接受正常的ART治疗方案,并增加2个多替格拉韦和米拉沃,后者已被证明可作为潜伏期逆转剂(LRA)。
- 在第三组中,Diaz给予增强抗逆转录病毒治疗和HDAC抑制剂烟酰胺(维生素B3),以增强诱导HIV脱离潜伏期的努力。
- 第4组接受金粉金糠强化抗逆转录病毒治疗,金糠糠因其氧化还原特性在治疗其他疾病方面显示出前景。
- 第5组接受部分强化抗逆转录病毒治疗(只是多替格拉韦),随后接受治疗性树突状细胞疫苗以增强抗艾滋病毒免疫。
- 最后,第6组接受了范围:部分强化ART,烟酰胺作为HDAC抑制剂,金粉金糠蛋白和治疗性疫苗。
<s:1>圣保罗病人来自第6组。
在停止所有抗逆转录病毒治疗近一年半后,他仍检测不到病毒DNA。即便如此,他的艾滋病病毒再次出现也不是史无前例的。据记者特里·怀尔德(Terri Wilder)的采访,给迪亚兹带来希望的是,他的艾滋病毒抗体水平正在下降。
这表明没有抗原(HIV)刺激它们的产生,这反映了在其他2名治愈患者中观察到的情况。然而,在6个月前接受抗逆转录病毒治疗的HIV阳性婴儿中也观察到低抗体或未检测到抗体,包括“密西西比婴儿”,其感染在缓解多年后复发。
重要的是,这位
这对即使是最兴奋的人也发出了强烈的警告,并暗示了
我们至少知道,在临床试验之前,他没有表现出“精英控制”的特殊特征,或者在不使用抗逆转录病毒治疗的情况下自发控制艾滋病毒感染的能力。HIV精英控制者在没有抗逆转录病毒治疗的情况下抑制病毒的惊人能力尚不完全清楚,但似乎是免疫系统遗传优势的一个方面,尤其是人类白细胞抗原(HLA)等位基因,或者可能是将前病毒DNA隔离到基因组的非转录区域,以及其他可能性。
然而,这位<s:1>圣保罗病人正在接受抗逆转录病毒治疗,并且经历过短暂的病毒血症,这意味着他不太可能是一位精英控制者。
时间和研究将继续阐明我们的认识。迪亚兹和他的团队已经获得了第二项更大规模的临床试验的资金。但是现在,在这第34届世界艾滋病日,我们庆祝希望的可能性、进步的承诺和一个人在抗击艾滋病毒方面取得的令人兴奋的成功。
*柏林病人蒂莫西·雷·布朗(Timothy Ray Brown)于2020年9月29日因白血病去世,尽管他在余生中一直治愈了艾滋病毒。由美国微生物学会提供引文:征服潜伏的艾滋病毒和结束艾滋病大流行的探索(2023年12月1日)检索自2023年12月1日https://medicalxpress.com/news/2023-12-quest-conquer-latent-hiv-aids.html此文件受版权保护。除为私人学习或研究目的而进行的任何公平交易外,未经书面许可,不得转载任何部分。内容仅供参考之用。