肠道菌群或肠道内的微生物群落,在消化和维持整体健康方面起着关键作用。因此,肠道菌群的任何紊乱都会对全身产生影响。肠道微生物将膳食成分代谢为有益脂肪酸(FAs),支持代谢和维持宿主体内稳态。
源自多不饱和脂肪酸(PUFAs)的代谢物,受植物乳杆菌等肠道微生物的影响,对炎症和免疫反应表现出强有力的影响。
操纵肠道细菌及其代谢物有望治疗代谢和炎症性疾病。然而,尽管肠道健康和健康趋势取得了进展,但控制微生物衍生代谢物免疫调节特性的确切机制仍然难以捉摸。
为了弥补这一差距,由东京科学大学的Chiharu Nishiyama教授领导的一组研究人员使用体外和体内小鼠模型进行了一系列实验,以了解细菌产生的FAs如何调节免疫反应。
Nishiyama教授解释了他们在免疫学前沿发表的工作背后的基本原理,他说:“PUFAs经历了肠道细菌所拥有的酶的代谢转化,如羟基化和饱和。近年来,人们发现这些肠道细菌代谢物具有多种有益的生理作用。
“在这项研究中,我们利用小鼠来源的免疫细胞研究了多种FA代谢物的活性。”
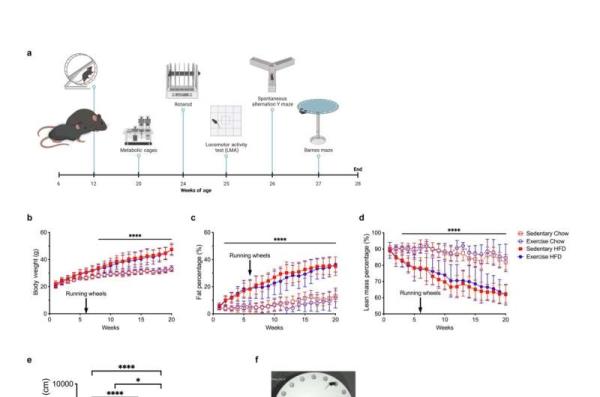
为此,研究人员使用抗原刺激的脾细胞来引发增强的免疫反应。随后,他们研究了不同多不饱和脂肪酸(PUFA)衍生物的影响,重点研究了亚油酸(一种普遍存在的膳食脂肪酸)的代谢物。
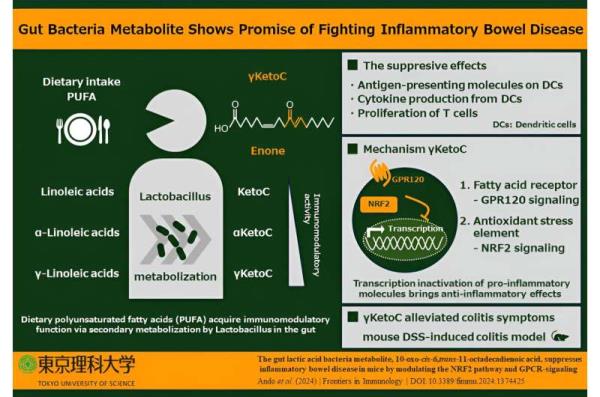
他们的研究结果显示,KetoC、αKetoC、gKetoA和gKetoC (LA的烯子衍生物)显著降低了白细胞介素2的水平,白细胞介素2是触发免疫细胞扩张和炎症的关键蛋白。然而,原始的未转化形式的PUFAs并没有表现出相同的免疫抑制作用,这强调了细菌转化在激活其免疫调节特性中的关键作用。
此外,他们还观察到,氙(一种功能基团)FAs也抑制了t细胞增殖和树突状细胞活化的延长,这可能导致炎症和自身免疫性疾病。这种抗炎作用在gKetoC中最为明显。因此,研究人员旨在揭示gKetoC发挥其免疫抑制作用的分子机制。
此外,先前的研究表明G蛋白偶联受体(gpcr)和转录因子NRF2参与抗氧化反应,这是由几种FA代谢物介导的,而gpcr和NRF2参与树突状细胞中gKetoC的作用在很大程度上是未知的。
为了阐明这些蛋白在gketoc介导的免疫反应中的作用,研究人员评估了抗原刺激和gketoc处理的树突状细胞释放的炎症细胞因子的水平。他们的研究结果表明,gKetoC刺激NRF2信号通路,从而抑制炎症细胞因子的产生。
此外,gpcr信号还以nrf2依赖的方式抑制树突状细胞中炎症细胞因子的产生。这揭示了控制gKetoC免疫调节作用的潜在分子轴。
为了进一步在体内验证他们的发现,研究人员使用了炎症性肠病的小鼠模型,并通过gKetoC治疗检查了免疫和炎症反应。他们发现,gKetoC治疗显著减少了结肠纤维化引起的组织损伤,减少了结肠炎引起的体重下降,并改善了粪便评分。
此外,接受治疗的小鼠显示上皮细胞破坏和溃疡减少,免疫细胞浸润减少,血清炎症因子水平降低。值得注意的是,NRF2缺失的模型在gKetoC治疗后,结肠炎诱导的组织损伤明显恢复。
总的来说,本研究揭示了gKetoC减轻抗原诱导的肠道炎症的潜在机制。需要进一步的研究来了解gKetoC、gpcr信号传导和NRF2通路之间的复杂相互作用,并揭示gKetoC介导其抗炎作用的其他潜在靶点。
然而,抗炎FA代谢物在治疗肠道炎症性疾病和维持肠道健康方面具有治疗前景,作为益生元或益生菌制剂。
西山博士分享了她的结论,他说:“我们的研究结果表明,膳食油的化合物被肠道细菌转化为有用的代谢物,具有抗炎作用。
“通过在个体、细胞和基因水平上进行详细的分析,我们希望了解我们每天吃的食物是如何影响免疫细胞的功能的,以及如何将这些影响作为预防和减轻炎症性疾病的目标。”
总之,虽然已知细菌PUFA代谢物的有益作用,但本研究确定gKetoC是在结肠炎小鼠模型中发挥保护作用的代谢物。从长远来看,这些发现可以帮助改善炎症性疾病患者的生活质量,并增加基于这些微生物代谢物开发功能性食品、补充剂和营养保健品的可能性。
此外,研究人员还推测,这些进展可能有助于识别和开发能够预防或减轻免疫相关疾病的化合物。
更多信息:Miki Ando等,肠道乳酸菌代谢物,10-氧-顺式-6,反式-11-十八烯二酸,通过调节NRF2通路和gpcr信号抑制小鼠炎症性肠病,Frontiers in Immunology(2024)。DOI: 10.3389/ fimmune .2024.1374425期刊信息:免疫学前沿由东京科学大学提供引文:肠道细菌代谢物显示出对抗炎症性肠病的希望(2024,5月7日)检索自2024年5月7日https://medicalxpress.com/news/2024-05-gut-bacteria-metabolite-inflammatory-bowel.html本文受版权保护。除为私人学习或研究目的而进行的任何公平交易外,未经书面许可,不得转载任何部分。内容仅供参考之用。